執筆者

霜田雅之(国立健康危機管理研究機構 国立国際医療センター 膵島移植診療科長、膵島移植センター長/国立国際医療研究所 膵島移植企業連携プロジェクト プロジェクト長)
![]() プロフィール
プロフィール
1998年京都大学医学部卒業、外科医として修練したのち2008年京都大学大学院医学研究科修了、2007年より米国ベイラー大学メディカルセンター研究員を経て2012年より国立国際医療研究センター研究所膵島移植プロジェクト長(現:国立健康危機管理研究機構国立国際医療研究所 膵島移植企業連携プロジェクト長)、2022年4月より現職
![]() 休日の過ごし方
休日の過ごし方
読書、子供の相手、たまにスポーツやキャンプ
![]() 研究室や運営するホームページ
研究室や運営するホームページ
http://www.ncgm.go.jp/080/suitou.html
はじめに
1型糖尿病根治の治療法として期待される「膵島移植」ですが、「ドナー不足」と「免疫抑制剤が必要であること」が課題となっています。私たちはその課題を克服するため、大量、安価に入手可能なブタの膵島を特殊なカプセルで封入した「バイオ人工膵島」の開発を進めています。
バイオ人工膵島移植の基礎およびこれまでの発展経緯
20世紀に飛躍的に発展した臓器移植・細胞移植は各種臓器が機能しなくなった患者さんに対する根治的治療として大いに役立ってきました。自分のインスリンがほとんど出なくなってしまった1型糖尿病患者さんに対する膵島移植もそのひとつです。しかし、ドナー数は患者さんの数に比べるととても少なく、移植数は限られているのが現状です。
そこで、ドナーから提供される臓器に代わる、移植に適した細胞・臓器の研究が進んでいます。その中で、家畜であり大量に入手可能なブタ(異種動物)の臓器を使って患者さんに移植する「異種移植」がドナー不足解消の切り札として期待されています。この場合、病原体のいない特殊なブタ(医療用ブタ)を使うことにより感染症を防ぎます。ただし、ヒト同士の臓器移植の場合と同様に、拒絶反応を防ぐための免疫抑制剤が必要です。膵島移植の分野でも、ブタ膵島を移植用に用いる研究が進んでいます。
国内外の研究開発の現状
このような糖尿病に対するブタ膵島移植は、異種移植の分野でも特に進んでおり、すでに数十年前から海外では臨床試験が行われています(表1)。
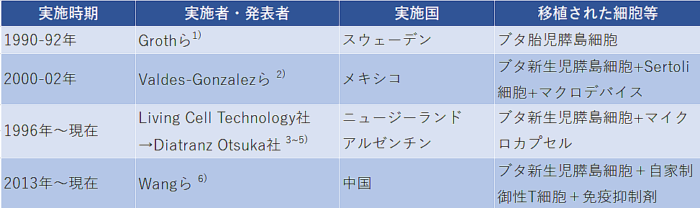
(表1)海外で行われた主なブタ膵島移植の臨床試験
ただし日本ではまだ1例も行われていません。近年では主に特殊な半透過性のカプセル(細胞を包んで隔離することで免疫反応は抑制するが、酸素や栄養素、インスリンは自由に通過する)にブタ膵島を封入して移植し、免疫抑制剤を使用しない形で実施されてきました。私たちはこの特殊カプセルに包まれたブタ膵島のことを「バイオ人工膵島」と呼んでいます(図1)。
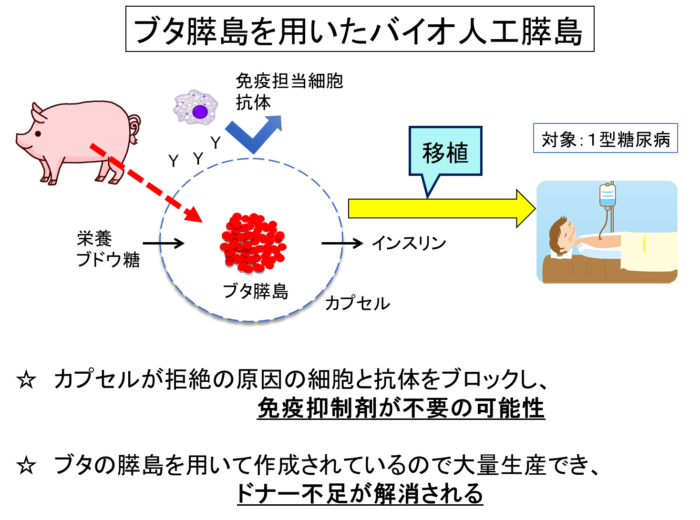
(図1)バイオ人工膵島移植の模式図
図中の抗体とは、患者さんのリンパ球で作られる特殊なタンパク質で、移植された細胞を異物と認識して攻撃し、破壊してしまう物質です。
これまでのところバイオ人工膵島を移植された患者さんにブタ由来の感染症は無いとされており、安全性は高いと考えられます。免疫抑制剤を使用しないので、その副作用もありません。治療効果としては、インスリン注射が不要になるまでの効果にはならなくてもインスリン注射量を減らし低血糖発作を軽減しつつHbA1cも改善するなど血糖安定化効果が認められています。
なお、現行のヒト同士の膵島移植と同様にカプセルなしで移植し、免疫抑制剤を使用する方法も研究されており、霊長類モデルでは1年以上血糖値を正常化することに成功しています1)。この方法も有望ですが、我々はカプセル化膵島の利点が大きいと考えています。
今後の展望と課題
私たちはいまだ日本では実現していない、ブタ膵島を用いた「バイオ人工膵島」の1型糖尿病患者さんへの移植治療を目指しています。そのためには、新薬の開発と同様に、患者さんに移植する前に安全性や有効性について動物実験を中心に詳細に調べる必要があります。また多くの患者さんに使ってもらうためには製薬企業が製剤化して事業化する必要もあります。
参考文献
1) Groth CG, Korsgren O, Tibell A, et al: Transplantation of porcine fetal pancreatic to diabetic patients. Lancet 344; 1402–1404: 1994
2) Valdes-Gonzalez RA, Dornates LM, Garibay GN, et al: Xenotransplantation of porcine neonatal islets of Langerhans and Sertoli cells: A 4-year study. Eur J Endocrinol 153: 419–427: 2005.
3) Elliott RB, Escobar L, Tan PL, et al: Live encapsulated porcine islets from a type 1 diabetic patient 9.5 yr after xenotransplantation. Xenotransplantation 14; 157–161: 2007.
4) Matsumoto S, Tan P, Baker J, et al: Clinical porcine islet xenotransplantation under comprehensive regulation. Transplant Proc 46; 1992–1995: 2014.
5) Matsumoto S, Abalovich A, Wechsler C, et al: Clinical benefit of islet xenotransplantation for the treatment of type 1 diabetes. EBiomedicine 12; 255-262: 2016.
6) Wang Y, Lei T, Wei L, Du S, Girani L, Deng S. Xenotransplantation in China: Present status. Xenotransplantation. 2019 Jan;26(1):e12490.