1型糖尿病の患者・家族や支援者のみなさんと東京工業大学生命理工学院教授の粂昭苑先生の研究室を訪問し、お話をうかがいました。大学進学を目指す高校生(患者)や医療関係者のほか、研究室訪問の開催をご支援いただいた大塚商会の方も参加してくださり、バラエティに富んだ参加者で様々な質問が飛び交った「第9回 患者が行く!研究室訪問」となりました。
粂先生の研究については研究概要書をご覧ください。
なお、本事業は大塚商会ハートフル基金の助成を受けて開催することができました。
目次
-
- (動画)
- 粂先生からのメッセージ
(前編)
(後編)
粂先生からのメッセージ
研究室訪問(前編)
膵臓の研究をはじめたきっかけ
東京工業大学に来るまでは熊本大学に13年ほど在籍したが、そこでヒトiPS細胞の研究を立ち上げました。博士課程在学中から発生(からだや臓器がどうやってできるか)についてアフリカツメガエルをつかって研究をしていました。博士号をとってから約10年間ポスドクとして日本で研究をしていましたが、アメリカに留学したことを1つの契機として、膵臓の研究をするようになりました。留学先の研究室の先生も、もともとアフリカツメガエルの研究者でしたが、お子さんが1型糖尿病の患者であったことから、膵臓発生や1型糖尿病についての研究を始めたばかりでした。膵臓の研究について調べてみるとあまり研究が進んでいなかったのが、新しいことをしたかったというのもありました。
現在東京工業大学に来て3年目。昨年初めての研究室の学生が卒業しました。現在21名程度の学生が研究室に在籍しています。
これまでの研究内容
どのようにして膵臓ができるのか、発生について研究を始めたころは解明されていませんでした。これを知って初めて作ることができると思うので、まずは膵臓の発生について研究を始めました。
再生にはいくつかの方法が考えられます。例えば、通常では組織の損傷修復には、それぞれの組織で眠っている幹細胞によって再生されます。しかし、再生しやすい組織もあれば、しにくい組織もあります。膵臓は再生しにくい組織です。体内から膵臓の幹細胞を取り出して増やすことは難しいと考えられています。
そこで、多能性幹細胞(ES細胞やiPS細胞)を使えば増やすことは難しくないだろうと考え、以前発生の研究をしていたのでやりやすいということもあり、多能性幹細胞で研究を始めてみました。
 まず、正常な発生過程では細胞がどのような遺伝子を発現させてβ細胞になるのかの過程を見るのが一番よいだろうと考えました。これまでの研究から、膵臓の前駆細胞(膵臓になることが決まっている細胞)ではたらく遺伝子(PDX-1)など様々な遺伝子が発現していることがわかっています。こういった遺伝子を目印に膵臓の前駆細胞を追跡することで、どのように前駆細胞が膵臓β細胞に分化していくのかが分かってきました。マウスだけでなく、ヒトの細胞でもどのような遺伝子がかかわっているか、についても研究をしています。
まず、正常な発生過程では細胞がどのような遺伝子を発現させてβ細胞になるのかの過程を見るのが一番よいだろうと考えました。これまでの研究から、膵臓の前駆細胞(膵臓になることが決まっている細胞)ではたらく遺伝子(PDX-1)など様々な遺伝子が発現していることがわかっています。こういった遺伝子を目印に膵臓の前駆細胞を追跡することで、どのように前駆細胞が膵臓β細胞に分化していくのかが分かってきました。マウスだけでなく、ヒトの細胞でもどのような遺伝子がかかわっているか、についても研究をしています。
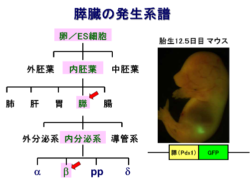
どういう道筋をたどったらβ細胞になるかを発生系譜といいます。
未分化の細胞をβ細胞へと誘導する因子はなにかを調べました。
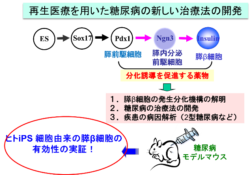
最終目標はβ細胞を作ることですが、まずは膵臓の細胞を作ることを目指しました。膵臓になるための遺伝子PDX-1に、PDX-1が発現すると緑の蛍光タンパク質の遺伝子をつなげ、前駆細胞が蛍光を出すようにしました。緑に光っていれば膵臓ができていることがわかります。緑に光る細胞がたくさん増える条件を調べていきました。
膵臓前駆細胞まで到達したあとは、内分泌前駆細胞への分化を促す化合物を調べました。ただ、内分泌前駆細胞を通り過ぎてしまってβ細胞まで分化していくので、実際インスリンを目印とした方がうまくいきました。
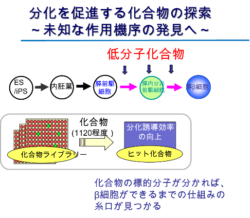
加える成長増殖因子は私たちがわかっているものだと数が多くないので、たくさん試してみようと思い、約1120種類の化合物を細胞に加えて培養しました。
いい結果が得られた化合物はいくつかありました。おもしろいことに、その化合物の働きは「β細胞を作らせない仕組みを阻害する薬物」だったのです。
いい結果が得られた化合物を入れてマウスのES細胞から分化した膵島細胞を糖尿病マウスに移植すると、マウスの血糖値が改善したという結果が得られました。次はヒトのiPS細胞でもできるかを確認していく必要があります。
生まれるまでマウスは20日、ヒトは10か月かかるように、マウスと違ってヒトは時間がかかります。そのため、マウスの実験から入った方が早く結果が出ます。ただしマウスでわかったことがすべて100%ヒトに応用できるとは言えません。たまには若干違う仕組みがあります。
さらに、培地が大事だということもわかってきました。培地は細胞に栄養を補給してくれます。私たちが食べ物に気をつけるのと同じことです。培地の組成は重要だということがわかってきました。
そもそもなぜそのような研究をし始めたかというと、ES細胞やiPS細胞にもいろいろな細胞株があり、それぞれ若干性格が異なります。よく増える細胞とゆっくり増える細胞、なかなか分化しない細胞、よく分化する細胞…。分化効率が悪く未分化の細胞が残ってしまうと、あとから悪さをして腫瘍を作る可能性がありますので、未分化の細胞を殺すかすべて分化させるようにしなければなりません。
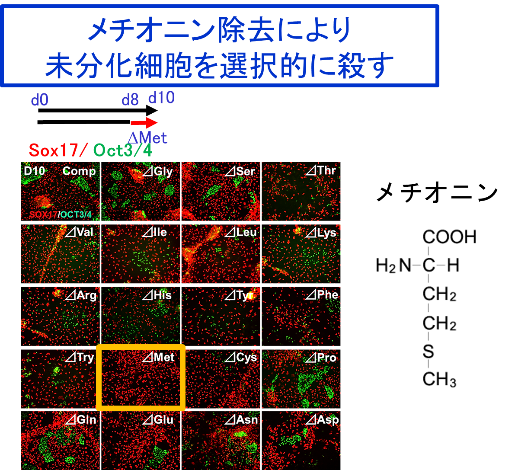
そこで、20種類あるアミノ酸を1つずつぬいた培地を用意しました。
するとおもしろいことに、メチオニンを除去すると、未分化細胞を選択的に殺すことがわかりました。これはおもしろいと思い、なぜそのようになるのかを調べました。
高校2年生だとアミノ酸はもう勉強していますよね。メチオニンはタンパク質の開始コドンです。メチオニンはいろんなタンパク質にメチル基を与えるという大事な役割があります。これをメチル化といいます。
 たとえば、エピジェネティクスというのは知っていますか。ゲノムというのは遺伝情報。エピという文字がついているので遺伝情報を超えたものという意味です。遺伝情報は同じだけれども、どの遺伝子を発現するかを決めるためにDNAやヒストンにいろいろなマークをつけます。使うものにはしおりをつけて分かりやすくし、使わないものは引き出しの中にしまってしまうというようなイメージです。たとえば、筋肉ではこの遺伝子を不活性化させる、膵臓ではこの遺伝子を活性化させる、というときにDNAやヒストンなどがメチル化されます。
たとえば、エピジェネティクスというのは知っていますか。ゲノムというのは遺伝情報。エピという文字がついているので遺伝情報を超えたものという意味です。遺伝情報は同じだけれども、どの遺伝子を発現するかを決めるためにDNAやヒストンにいろいろなマークをつけます。使うものにはしおりをつけて分かりやすくし、使わないものは引き出しの中にしまってしまうというようなイメージです。たとえば、筋肉ではこの遺伝子を不活性化させる、膵臓ではこの遺伝子を活性化させる、というときにDNAやヒストンなどがメチル化されます。
私たちは、メチオニンを最初だけ除いた培地で数時間培養すると、iPS細胞が分化しやすくなること、最初はそんなに大きな違いでは無いのですが、最終的にβ細胞になりやすくなることが分かりました。
将来再生医療を用いた糖尿病の新しい治療法の開発
このような研究から、先ほどお話しした化合物が糖尿病の治療薬につながるかもしれないということで研究をしています。体内にある膵臓の前駆細胞を、化合物を例えば経口薬で飲むことで、より分化させる飲み薬が見つかるかもしれません。幹細胞は移植できるようなものをつくることももちろんですが、発生機構を調べたり、治療法の開発にも活用できます。
2型糖尿病にも遺伝的因子があることがわかっていますが、直接の因果関係がわかっていない遺伝子も多いです。一人一人のDNAの塩基配列の違いを調べることで、2型糖尿病に関連している遺伝子が見つかってきています。それをもっと深く研究するために、例えば、こうした遺伝子について、iPS細胞で遺伝子を改変したりすることによって、分化した膵臓β細胞が糖尿病になりやすくなるかを調べるような研究もしています。
移植に使える細胞の研究については、フラスコの底に貼りついているとたくさん培養するのは難しいので、貼りついていない状態で増せるようにしています。また、培養して、完全にβ細胞になってから
移植したほうがいいのか、前駆細胞のうちに移植したほうがいいのか、など、どの段階で移植するといいのかも試しています。マウスやマーモセットへの移植手術をしています。
2型糖尿病関連遺伝子はたくさん報告されています。そのうちの1つを、患者さんからいただいた細胞で、他の大学で共同研究しています。患者の細胞と正常の細胞を解析・比較してどこが異なるのかなどの研究もしています。
用語集
・アフリカツメガエル
発生の実験でよく使われるカエル。体の表面が粘液に覆われ、ぬるぬるしている。
・発現
遺伝子の情報をもとにタンパク質を合成すること。
・遺伝子
遺伝情報をもつDNAの一部分。1つの遺伝子から1種類のタンパク質が合成される。
・DNA(デオキシリボ核酸)
遺伝子を保持している物質。核に多く含まれる。
・ヒストン
DNAが巻き付いているタンパク質。DNA分子を折り畳んで核内に収納する役割をもつ。
・リプログラミング
分化した細胞を未分化の状態に戻す、または異なる細胞へ分化させること。
・科研費
科学研究費補助金の略
・アミノ酸
タンパク質を構成する物質。ヒトの場合は20種類のアミノ酸ですべてのタンパク質が構成されている。
・タンパク質
アミノ酸が多数結合した物質。
・エピジェネティクス
多細胞生物の体細胞において細胞核に含まれる遺伝子の構成は基本的に生涯を通して同じものであるが、各細胞は必要に応じて発現させる遺伝子を切り替えて利用している。そのような後天的な遺伝子発現の制御の変化を一般にエピジェネティクスと呼び、DNAのメチル化修飾やヒストンタンパク質の化学修飾などによって制御されることが分かってきている。(wikipediaより)
(後編へ続く)