汎例:*1…注釈番号 1)…参考文献番号
執筆者
後藤昌史(東北大学医学系研究科移植再生医学分野 教授)
![]() プロフィール:
プロフィール:
1993年東北大学医学部卒業、外科医として修練したのち2000年東北大学大学院医学博士号取得、その後カロリンスカ研究所及びウプサラ大学研究員を経て2015年より現職
![]() 休日の過ごし方:研究、テニス、読書
休日の過ごし方:研究、テニス、読書
![]() 研究室のホームページ:
研究室のホームページ:
http://www.med.tohoku.ac.jp/about/laboratory/094.html
http://www.tx-regenerativemed.med.tohoku.ac.jp
http://www.tx-regenerativemed.med.tohoku.ac.jp/IsletsProject/islets.html
はじめに
1型糖尿病患者の多くは頻回の自己血糖測定とインスリン療法によって血糖コントロールが可能ですが、一部の患者は深刻な低血糖性昏睡による致死の危険に常にさらされています。さらに近年に至り、インスリン療法ではその厳格な使用にもかかわらず、血管病変に基づく腎不全、失明、神経障害、心筋梗塞、脳卒中といった糖尿病長期合併症の併発を完全には阻止できないことが明らかとなってきました。わが国においても、昨今の人口高齢化に伴い、透析導入患者に占める糖尿病患者の割合は年々増加しており、またその予後が他疾患を原因とするものよりはるかに不良であることが報告されています。したがって、医療的側面および長期的な医療費削減を踏まえた社会的側面からも、これら糖尿病患者を治癒へ向かわせる根治療法、すなわち膵β細胞の置換療法の確立が急務であると考えられています。
膵島移植の基礎およびこれまでの発展経緯
膵臓は、消化酵素を分泌して消化吸収を助ける外分泌細胞と、インスリンやグルカゴンなどのホルモンを分泌して血糖調節を行う内分泌細胞との、2種類の全く働きの異なる細胞群により構成されています。膵内分泌細胞群は膵臓全体の約99%を占める膵外分泌組織の中に点々と散在しており、その様子から膵島という名称がつけられています。膵島は直径が約 0.1〜0.4 mmの球状の細胞塊で、成人1人あたりの膵臓の中に約100万個存在しているといわれています。膵島はα細胞·β細胞·δ細胞·PP細胞より構成されていますが、60 – 70%はβ細胞が占めています。β細胞は、血糖が上昇した場合に血糖を低下させるホルモンであるインスリンを分泌します。反対に血糖が低下しすぎた時には、α細胞から血糖を上昇させる働きがあるグルカゴンが分泌されます。このように、膵島はそれ自体で血糖を感知し調整を行うことが可能です。
膵島移植とは、臓器提供者の膵臓からこの膵島を抽出し、血糖コントロールが困難である重症糖尿病患者に対し点滴の要領で移植を行う低侵襲*1な細胞移植療法のことです1)。同じ目的で実施される膵臓自体の移植である膵臓移植と比べて、安全、簡便、低侵襲であり、患者に優しい治療法であるため、今後の糖尿病治療の中心を担っていくと期待されています。
膵島移植の主な目的は、インスリンの強化療法によっても血糖コントロールが困難である重症1型糖尿病患者の血糖値を安定化させ、それにより低血糖発作を解消することです。それにより副次的に糖尿病合併症を阻止し、究極的には患者の生活の質を向上させるためインスリンからの離脱を目指します。膵島移植の適応となる患者は膵臓のインスリン分泌能が枯渇しており、糖尿病学会専門医らのエキスパートによる治療によっても血糖のコントロールが困難であるインスリン依存性の重症1型糖尿病患者です。膵島移植の禁忌としては、重症感染症や悪性腫瘍の治療中などが挙げられますまたアルコール中毒や重症肥満の患者も適応外となります。
*1 侵襲…「手術」「医療処置」などの外部からの刺激による身体に対する負担や影響
国内外の研究開発の現状
膵島移植の臨床成績は当初満足できるものではありませんでしたが、2000年のエドモントンプロトコール(免疫抑制療法から膵島障害性のあるステロイド剤を排除しmTOR*2を新たに導入、複数ドナー*3から一人の患者へ膵島移植を実施、それまでの培養膵島に代わり膵島分離直後の新鮮膵島を移植に使用)の報告を契機に1)、膵島分離技術2) 3)や免疫抑制療法の改良4)が積極的に推し進められ、近年大きく改善されてきています。抗胸腺抗体*4および炎症性サイトカイン阻害剤*5の導入を柱として、北米を中心に実施された第III相多施設共同臨床試験の結果が近年報告され5)(図1)、膵島移植が重症1型糖尿病患者の低血糖発作解消に有効な治療法であることが実証されたことは特記に値します。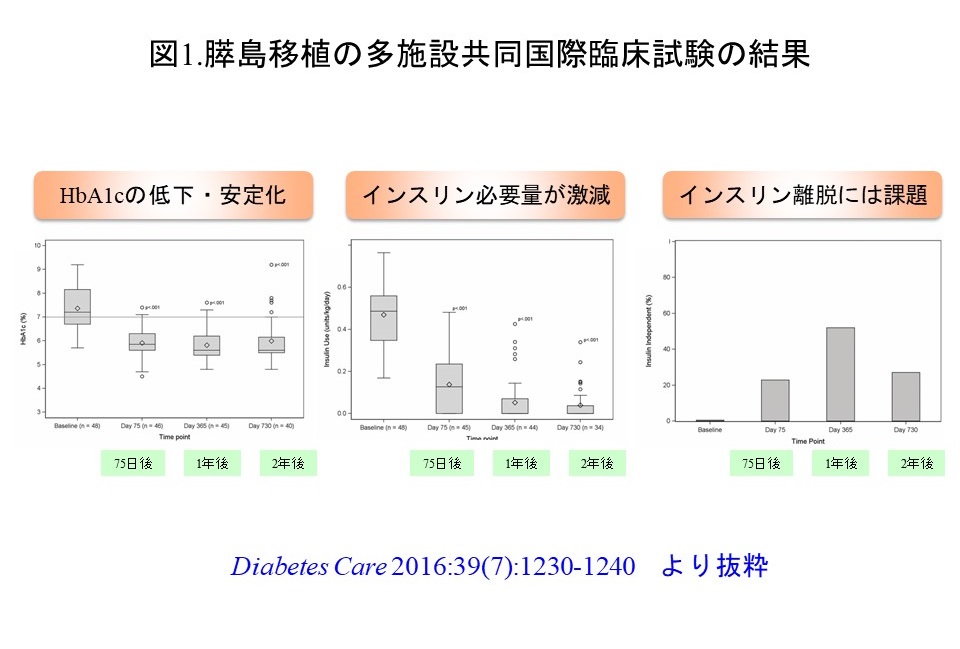
わが国で膵島移植を希望する場合は、必要検査データをそろえた上で、日本膵・膵島移植研究会が設置する膵島移植適応検討委員会に主治医より申請を行う必要があります。適応があると認められた場合には、日本膵・膵島移植研究会にレシピエント*6登録を行い膵島の提供を待つことになります。日本膵・膵島移植研究会が認定し、膵島移植を行うことが可能な施設が現在全国に11 (北海道大学、東北大学、福島医科大学、国立健康危機管理研究機構 国立国際医療センター、信州大学、大阪大学、京都大学、岡山大学、徳島大学、福岡大学、長崎大学)存在しますが、現行のルールでは患者が複数の施設に登録を行うことも可能です。2020年4月にようやく脳死ドナーおよび心停止ドナーからの同種膵島移植が保険収載*7されましたが、保険診療に際し厚労省が新たに施設基準を設定したため(厚労省保医発0305第3号第76の2)、上記11認定施設のうち厚労省基準を満たした施設から順次保険診療を開始していく予定です。留意すべき点として、同種(ヒトからヒトへの)膵島移植は2014年に施行された“再生医療等の安全性の確保等に関する法律”が規定する第一種医療技術に組み込まれたため、これまで国内で治療を実施する際は特定認定再生医療等委員会の承認を得た上で、上記法律に準拠することが必須となっていましたが、保険診療となった後も当面の間、例外的に上記法律への準拠が求められることとなりました。
*2 mTOR阻害剤…細胞の増殖に関わるmTORというタンパク質に選択的に結合することにより免疫細胞の機能を抑制する薬
*3 ドナー…移植の際の臓器提供者
*4 抗胸腺抗体…免疫細胞の教育を担当する重要な器官である胸腺の機能を阻害する強力な抗体
*5 炎症性サイトカイン阻害剤…炎症反応を引き起こす引き金となる強力な体内物質の機能を落とす薬剤
*6 レシピエント…移植の際の臓器受容者
*7 保険収載…保険適用になること
今後の展望と課題
膵島移植は、血糖コントロールに苦しむ重症1型糖尿病患者にとり、まさに理想的な患者に優しい治療法です。しかし、極端に脳死ドナーが少ないわが国の特殊事情を考慮すると、今後の膵島移植の方向性として、異種膵島*8を使用するバイオ人工膵島移植やES*9・iPS*10細胞を使用する再生医療といった選択肢も十分視野に入れ、そのための高性能な免疫制御デバイス*11の開発や移植部位の至適化に関する技術革新が極めて重要です。
移植部位に関しては、門脈*12を介し肝臓内へ移植する方法が現行の世界標準ですが、今後ES・iPS細胞由来の膵島やブタ膵島などを移植する際に潜在的に起こり得る腫瘍や感染症といったリスクを鑑みると、超音波検査機で外来フォローすることができ、万一のリスク発生時に移植膵島を容易に摘出することが可能である皮下への移植が好ましいと考えられます。さらに皮下膵島移植は低侵襲であり、複数回の移植を安全に行えるといった様々な利点を有していますが、皮下は血管に乏しく、移植膵島に十分な酸素や栄養を供給することができないため、これまで実現に至りませんでした。この課題を克服するには、移植部位となる皮下の血管床*13を効果的に構築することが重要であり、Basic fibroblast growth factor*14(塩基性線維芽細胞増殖因子)やHepatocyte growth factor*15肝細胞増殖因子)が有効であることがこれまでに報告されてきましたが6)、これらのgrowth factor*16(増殖因子)は腫瘍化リスクや炎症惹起性*17を伴うため実用化には慎重とならざるを得ません。そこで筆者らは血管誘導作用を有するRGD基*18を豊富に含有する新規コラーゲン素材(リコンビナントペプチド:RCP)に着目し、これを移植部位である皮下に前留置することにより安全かつ効果的に新生血管床の構築が可能であり、移植膵島の生着*19を有意に促進することができました7) (2)。今後、こういった新しい皮下膵島移植法と免疫制御デバイスを組み合わせることにより、脳死ドナーや免疫抑制剤が不要である“次世代型膵島移植”の実現が期待されます。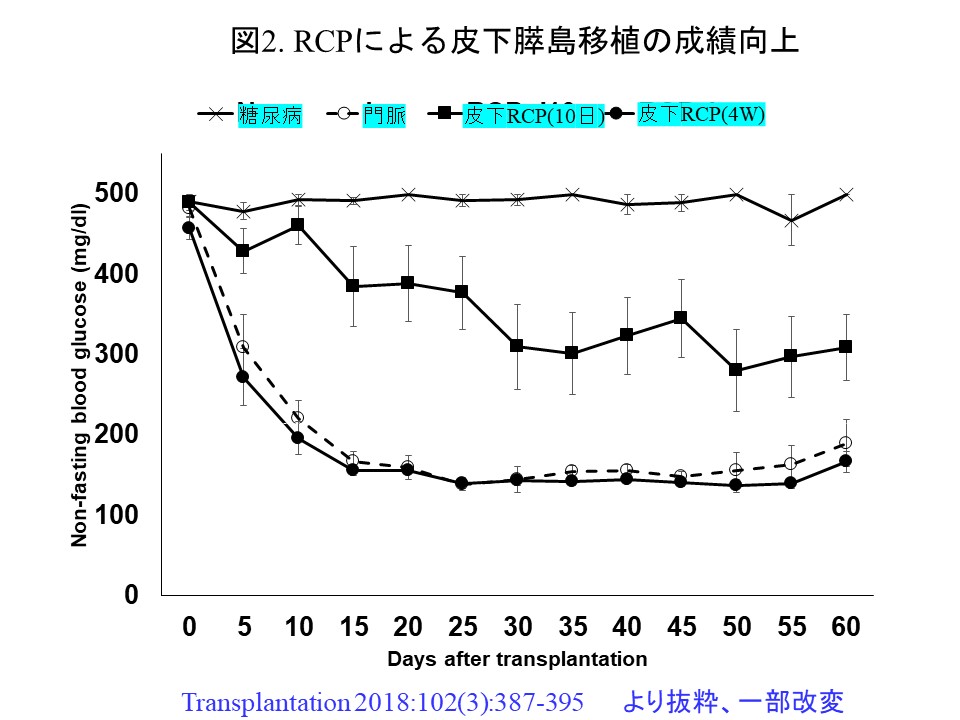
*8 異種移植…ヒト以外の動物からヒトへの移植
*9 ES細胞…embryonic stem cells(胚性幹細胞)
*10 iPS細胞…induced pluripotent stem cells(人工多能性幹細胞)
*11 免疫制御デバイス…インスリン、酸素、糖などは通過するものの抗体や血球などは遮断する能力を有する細胞を包むデバイス(膜やカプセル)のこと
*12 門脈…上腸管膜静脈と脾静脈が合流し肝臓へ繋がる部位の大血管
*13 血管床…移植された膵島細胞への栄養物質供与という重要な役割を可能とするような血管ネットワークのこと
*14 Basic fibroblast growth factor…既に褥瘡(床ずれ)の治療などで実際に使用されている細胞の成長を促す薬剤
*15 Hepatocyte growth factor…当初肝細胞の成長を促す薬剤として見つかりましたが、他の多くの細胞にも有効であることが判明している増殖因子
*16 growth factor…細胞の成長を促す強力な薬剤
*17 炎症惹起性…炎症を引き起こす性質
*18 RGD基…インテグリン(細胞膜にあるタンパク質で、細胞同士を接着する)の認識配列(Arg-Gly-Asp)であり、新生血管を呼び込む作用を有する
*19 生着…移植された細胞が正常に機能すること
参考文献
1)Shapiro AM, Lakey JR, Ryan EA, Korbutt GS, Toth E, Warnock GL, et al. Islet transplantation in seven patients with type 1 diabetes mellitus using a glucocorticoid-free immunosuppressive regimen. N Engl J Med. 2000;343(4):230-8.
2)Goto M, Eich TM, Felldin M, Foss A, Kallen R, Salmela K, et al. Refinement of the automated method for human islet isolation and presentation of a closed system for in vitro islet culture. Transplantation. 2004;78(9):1367-75.
3)Noguchi H, Ueda M, Hayashi S, Kobayashi N, Okitsu T, Iwanaga Y, et al. Ductal injection of preservation solution increases islet yields in islet isolation and improves islet graft function. Cell Transplant. 2008;17(1-2):69-81.
4)Bellin MD, Kandaswamy R, Parkey J, Zhang HJ, Liu B, Ihm SH, et al. Prolonged insulin independence after islet allotransplants in recipients with type 1 diabetes. Am J Transplant. 2008;8(11):2463-70.
5)Hering BJ, Clarke WR, Bridges ND, Eggerman TL, Alejandro R, Bellin MD, et al. Phase 3 Trial of Transplantation of Human Islets in Type 1 Diabetes Complicated by Severe Hypoglycemia. Diabetes Care. 2016;39(7):1230-40.
6)Kawakami Y, Iwata H, Gu YJ, Miyamoto M, Murakami Y, Balamurugan AN, et al. Successful subcutaneous pancreatic islet transplantation using an angiogenic growth factor-releasing device. Pancreas. 2001;23(4):375-81.
7)Uematsu SS, Inagaki A, Nakamura Y, Imura T, Igarashi Y, Fathi I, et al. The Optimization of the Prevascularization Procedures for Improving Subcutaneous Islet Engraftment. Transplantation. 2018;102(3):387-95.
おすすめの書籍や文献など
日本膵・膵島移植研究会ホームページ
http://plaza.umin.ac.jp/~jpita/index.html